Les médicaments dans l’environnement : sources, concentration et effets
Nathalie Ross, Ph.D., RAC
Collaboration spéciale

La persistance à la dégradation est une qualité recherchée dans le développement des médicaments. Par contre, cette persistance peut s’avérer problématique lorsque ces molécules se retrouvent dans l’environnement. Des recherches qui se sont intensifiées depuis une dizaine d’années montrent que certains médicaments se retrouvent dans les eaux de surface après un passage par un traitement d’eau usée. D’où proviennent ces produits pharmaceutiques mesurés dans l’environnement? Dans quelles concentrations les retrouve-t-on? Quel est leur effet sur l’environnement et la santé humaine?
L’excrétion par les patients : la principale source de médicaments dans l’environnement
Quoique les médicaments puissent atteindre l’environnement par plusieurs voies, la principale source est l’excrétion par les patients d’une fraction du médicament non utilisée par l’organisme (Figure 1). Or, il arrive que ces médicaments ainsi excrétés ne soient dégradés que partiellement par les traitements d’eau usées et atteignent ainsi les eaux de surface et les eaux souterraines (Cunningham et al., 2006).
Voies d’entrées des produits pharmaceutiques dans l’environnement
La principale préoccupation ne réside pas dans le volume de production de ces médicaments mais plutôt dans leur persistance à la dégradation et leurs effets très spécifiques à faibles doses sur les êtres vivants. Par exemple, les hormones synthétiques utilisées dans la fabrication de la pilule contraceptive amènent des effets féminisant chez les poissons dans des concentrations de 1 à 4 ng/l (Fent et al., 2006); soit l’équivalent de moins d’une pilule contraceptive dispersée dans une piscine olympique!
 Du milligramme dans les eaux usées au nanogramme dans les eaux traitées Du milligramme dans les eaux usées au nanogramme dans les eaux traitées
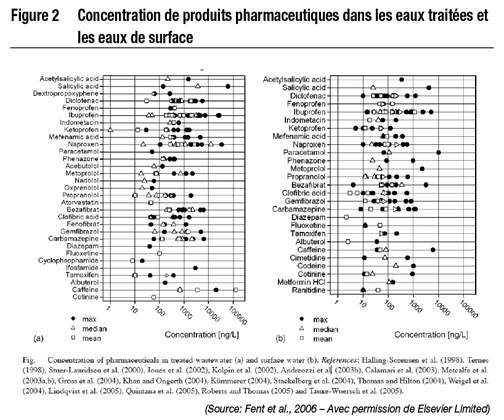
C’est dans les années 70 qu’une première étude américaine a rapporté des concentrations d’environ 1 µg/l dans les eaux traitées d’un médicament utilisé pour la réduction des gras sanguins (acide clofibrique) (Garrison et al., 1976). Depuis cette première étude, les méthodes de détection des molécules chimiques dans l’eau ont grandement évolué et des données plus récentes ont montré la présence de plus de 100 produits pharmaceutiques, dont des anti-inflammatoires, antiépileptiques, des régulateurs lipidiques, etc., dans les eaux usées traitées et les eaux de surface.
Test écotoxicologiques : manque de données sur les effets à long terme
Dans la communauté scientifique, il y a un consensus à l’effet que le risque sur la santé humaine de cette présence de médicaments dans l’environnement est faible. Par contre, on s’inquiète de la santé de la vie aquatique et terrestre de ces milieux. À l’heure actuelle, il est difficile de connaître les effets des médicaments sur ces organismes compte tenu du manque de données sur les effets à long terme (effets chroniques) (Cunningham et al., 2006).
 En effet, les méthodes couramment utilisées pour les tests écotoxicologiques reposent sur des expositions à court terme (expositions aigües) des médicaments sur des organismes tels les algues, le zooplancton et les poissons. Puisque dans la réalité, les organismes aquatiques peuvent être exposés durant toute leur vie à des rejets d’eaux usées, il apparaît crucial de valider des tests écotoxicologiques pour mesurer l’effet chronique d’une telle exposition. En effet, les méthodes couramment utilisées pour les tests écotoxicologiques reposent sur des expositions à court terme (expositions aigües) des médicaments sur des organismes tels les algues, le zooplancton et les poissons. Puisque dans la réalité, les organismes aquatiques peuvent être exposés durant toute leur vie à des rejets d’eaux usées, il apparaît crucial de valider des tests écotoxicologiques pour mesurer l’effet chronique d’une telle exposition.
Les volumes de fabrication ou d’importation sont la base du cadre réglementaire canadien
C’est en 1995 en Europe qu’une première norme environnementale à fait son apparition pour laquelle les médicaments vétérinaires devaient passer une batterie de tests écotoxicologiques avant leur approbation (EU Directive 92/18). Au Canada depuis 2001, les substances «nouvelles» sous la Loi sur les aliments et drogues sont sujettes à une évaluation environnementale avant leur approbation pour la fabrication ou l’importation au Canada (sous le Règlement de notification sur les substances nouvelles (RNSN) de la Loi canadienne de la protection sur l’environnement (LCPE)). On appelle substance «nouvelle» toute substance qui ne figure pas sur la liste intérieure des substances (LIS) – une liste exhaustive de toutes les substances connues qui sont ou ont déjà été offertes en vente sur le marché canadien.
Ce règlement prescrit les informations qui doivent être fournit par le fabricant de médicaments à Santé Canada et à Environnement Canada. L’étendue de ces informations, qui incluent l’identification chimique, des tests écotoxicologiques (p. ex. sur des poissons ou des algues) et des tests de mutagénécité (effets sur les gènes), dépend du volume de la nouvelle substance à être fabriquée ou importée au Canada sur une base annuelle (une fabrication ou importation de moins de 100 kg/an de la substance nouvelle est exemptée de l’obligation de soumettre une déclaration de substance nouvelle).
Avec ces informations en main, Santé Canada (SC) évalue le risque pour la santé humaine et Environnement Canada (EC) évalue le risque pour l’environnement. Une fois ce risque évalué, SC et EC communiquent avec le fabricant :
- dans le cas où la substance est soupçonnée non toxique : une lettre d’autorisation pour la fabrication/ importation de la substance ou,
- dans le cas où la substance est soupçonnée toxique : une imposition de conditions entourant la fabrication/importation de la substance, une demande de renseignements supplémentaires ou une interdiction de la fabrication/importation.
En collaboration avec l’industrie pharmaceutique, les scientifiques et les académiciens, Santé Canada et Environnement Canada développent une réglementation adéquate pour l’évaluation environnementale des produits pharmaceutiques qui serait basée sur un barème différent que les taux de fabrication ou d’importation annuels. Les parties prenantes du processus veulent éviter d’envoyer comme message que tous ces produits posent un risque à l’environnement.
Références
Cunningham, V.L., Buzby, M., Hutchinson, T., Mastrocco, F., Parke, N., Roden, N. 2006. Effects of Human Pharmaceuticals on Aquatic Life: Next Steps, Environmental Science and Technology, 40(11): pp. 3456-3462.
Fent, K., Weston, A.A., Caminada, D. 2006. Ecotoxicology of Human Pharmaceuticals, Aquatic Toxicology, 76: pp. 122-159.
Garrison, A.W., Pope, J. D., Allen, F.R. 1976. Analysis of Organic Compounds in Domestic Wastewater. In Keith, C.H. (Ed.), Identification and Analysis or Organic Pollutants in Water. Ann Arbor Science, Michigan, USA, pp. 517-566.
Health Canada. Consultation on the Development of Environmental Assessment Regulations Report, Environmental Impact Initiative, June 15, 2006, 19 pp.
Health Canada. Guide to New Substances Notification for Products Regulated Under the Food and Drug Act, Environmental Assessment Regulations Project Task Force, 7 May 2002, 28 pp.
|



